5 minuti per la lettura
Una molecola “truccata”, frutto di modellizzazione molecolare, sconfiggerà i batteri killer. Invisibili, sono i nemici dell’uomo fin dalle sue origini. Dalla notte dei tempi, i microbi, assai più delle guerre e delle carestie, hanno seminato vittime fra le popolazioni. La lotta della ricerca medica e scientifica per sconfiggerli è incessante, come ricorda la giornalista e autrice di Superquark e Ulisse, Barbara Gallavotti, che nel suo libro “Epidemie come difendersi. Tutto quello che dovreste sapere sui microbi”, racconta il drammatico inseguimento nella lotta alle epidemie che nel corso dei secoli hanno flagellato l’umanità. Dalla peste che fra il 1347 e il 1350 uccise quasi un terzo della popolazione europea, alla prima grande epidemia di sifilide che colpì Napoli nel 1495, la guerra invisibile dei patogeni non si è mai arrestata. La tubercolosi che nel XIX secolo segnò una vera e propria esplosione di vittime, fu responsabile, agli inizi dell’800, di una morte su quattro in Inghilterra e ancora, un secolo dopo, di una morte su sei in Francia.
Secondo una stima dell’Organizzazione Mondiale della Sanità (OMS), fra il 2000 e il 2017, cinquantaquattro milioni di vite sarebbero state salvate dalle terapie contro la tubercolosi. Cosa ci riserverà il futuro? Ciò che preoccupa maggiormente, dice Gallavotti, “è che ad uccidere oggi sono spesso le infezioni scatenate da batteri piuttosto comuni, contratte in ospedale o da persone indebolite, resistenti agli antibiotici”. Alcuni ceppi di batteri come Escherichia coli, che vive abitualmente nell’intestino umano, o come lo l’Enterococcus Faecium, che possono dare origine a meningite, polmonite o setticema, insieme a batteri del genere Pseudomonas, che rappresenta una minaccia per le vie urinarie o per i polmoni, nei pazienti affetti da fibrosi cistica, o ancora, lo Staphylococcus aureus, che può attaccare la pelle, i polmoni e le ossa, appaiono in alcuni casi incurabili. Il primo caso di Staphilococcus aureus resistente alla meticillina fu identificato nel Regno Unito nel 1962 e nel 1968 negli Usa, a breve distanza dall’inizio dell’uso del farmaco.
La guerra all’antibiotico resistenza non si è mai fermata ed oggi, una ricerca internazionale svolta dall’Istituto officina dei materiali del CNR con l’università di Cagliari in partnership con l’università di Oxford e il CNRS, pubblicata su Nature Communication, ha aperto il varco alla speranza di sconfiggere uno dei quattro batteri più pericolosi al mondo, lo Pseudomonas aeuroginosa. Partendo dagli studi sugli algoritmi di predizione dei modelli molecolari, iniziati oltre diciotto anni fa, Matteo Ceccarelli, scienziato e professore di biofisica all’Università di Cagliari, associato al CNR presso l’Istituto Officina dei Materiali (Iom) presso l’ateneo sardo, è riuscito a spiegare con il suo gruppo di ricerca il meccanismo grazie a cui i farmaci possono “raggirare” i batteri resistenti, attaccandoli efficacemente.
Oggi, spiega lo scienziato, «ci sono batteri che sono sempre più resistenti e sempre meno antibiotici risultano essere efficaci per debellarli. L’OMS stima che l’antibiotico- resistenza uccida 30 mila persone l’anno in Europa. Abbiamo compreso che la sfida non consisteva soltanto nell’identificare le molecole letali per i batteri, quanto piuttosto nel modellarle per raggiungere questi. I batteri Gram negativi (P. aeruginosa ed E. coli per esempio) sono protetti da una membrana esterna, abbastanza spessa, che impedisce agli antibiotici di raggiungere il loro interno, dove ci sono le proteine sensibili da bloccare.
Nel cercare nuovi antibiotici, le case farmaceutiche non sanno come trattare questa barriera esterna, la cui azione è evidente quando si passa dagli studi in vitro alle colture batteriche in vivo. Studiando l’interazione fra recettore e nutrienti, abbiamo trovato la chiave molecolare per penetrare attraverso la membrana esterna dello Pseudomonas aeruginosa».
La chiave contro l’antibiotico – resistenza.
La ricerca ha svelato il meccanismo attraverso il quale le molecole che trasportano nutrienti come il ferro, essenziale per la sopravvivenza dei batteri, riescono a utilizzare i recettori della membrana esterna, penetrando all’interno, e fornendo in tal modo, a chi disegna i nuovi antibiotici, gli strumenti per renderli efficaci e vincere l’antibiotico-resistenza.
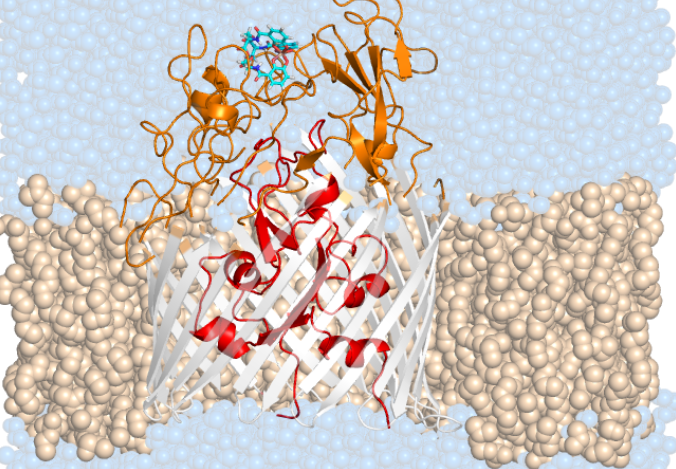
«Per comprendere come avviene il passaggio dei nutrienti abbiamo studiato una proteina, il recettore PfeA, che si trova sullo strato più esterno del batterio. Il recettore, prodotto e cristallizzato dall’Università di Oxford, è predisposto per l’ingresso della molecola Enterobactin, sintetizzata dal CNRS di Strasburgo, che lega uno ione ferro. Con modelli molecolari abbiamo capito come rendere questa molecola un “cavallo di Troia”: attaccandole un antibiotico, si consente il suo passaggio attraverso la membrana, senza toccare il meccanismo di ingresso e ingannando il batterio» – afferma lo scienziato.
La ricerca del team di Ceccarelli è stata sviluppata nell’ambito del consorzio pubblico di scienziati dell’IMI – Innovative Medicine Initiative-, l’iniziativa dell’Unione Europea volta alla collaborazione fra partner pubblici e privati, finalizzata ad affiancare le case farmaceutiche nella soluzione di sfide crescenti. «Comprendere come la molecola riesce a superare la membrana è stato il primo step. Il prossimo, sarà quello di attaccare alla molecola l’antibiotico». Matteo Ceccarelli racconta con orgoglio la genesi personale di questo risultato, per molti versi epocale. Dopo una laurea in Fisica all’Università di Cagliari nei primi anni ’90 e una laurea in biofisica alla Sissa di Trieste, da anni lavora sugli algoritmi di modellizzazione molecolare, «Quando ho iniziato c’era molto scetticismo su questi approcci per gli antibiotici»- ricorda.
Un PhD a Lione e un post-doc in Svizzera, seguiti da un’esperienza nei laboratori di una casa farmaceutica a Boston, uniti a una serie di fortunate coincidenze gemmate dai suoi interessi scientifici, lo hanno portato a guidare, nel 2013, una delle linee del progetto internazionale, coordinando cinque gruppi di ricerca, proprio per i suoi studi sul passaggio delle molecole dall’esterno all’interno delle membrane batteriche.
La qualità dell'informazione è un bene assoluto, che richiede impegno, dedizione, sacrificio. Il Quotidiano del Sud è il prodotto di questo tipo di lavoro corale che ci assorbe ogni giorno con il massimo di passione e di competenza possibili.
Abbiamo un bene prezioso che difendiamo ogni giorno e che ogni giorno voi potete verificare. Questo bene prezioso si chiama libertà. Abbiamo una bandiera che non intendiamo ammainare. Questa bandiera è quella di un Mezzogiorno mai supino che reclama i diritti calpestati ma conosce e adempie ai suoi doveri.
Contiamo su di voi per preservare questa voce libera che vuole essere la bandiera del Mezzogiorno. Che è la bandiera dell’Italia riunita.
ABBONATI AL QUOTIDIANO DEL SUD CLICCANDO QUI.
COPYRIGHT
Il Quotidiano del Sud © - RIPRODUZIONE RISERVATA